Stéarate de calcium Production et formation | Utilisations | Références | Menu de navigation1592-23-0100.014.97615324PubChemvue 3Dvue 3Dmodifierallemandanglais« Atomic weights of the elements 2007 »« Calcium stearate »ChemIDplus10.1002/14356007.a16_36110.1002/14356007.a28_001Preventing EfflorescenceBrevet U.S. 5,527,383
Composé du calciumAdditif alimentaireStéarate
tensioactifsacide stéariqueoxyde de calciumadditif alimentaire
| Stéarate de calcium | |
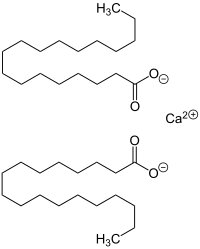 | |
| Identification | |
|---|---|
Nom UICPA | octadécanoate de calcium |
Synonymes | E470 |
No CAS | |
| NoECHA | 100.014.976 |
No CE | 216-472-8 |
No RTECS | WI3000000 |
PubChem | 15324 |
SMILES | [Ca+2].[O-]C(=O)CCCCCCCCCCCCCCCCC.[O-]C(=O)CCCCCCCCCCCCCCCCC , |
InChI | Std. InChI : InChI=1S/2C18H36O2.Ca/c2*1-2-3-4-5-6-7-8-9-10-11-12-13-14-15-16-17-18(19)20;/h2*2-17H2,1H3,(H,19,20);/q;;+2/p-2 Std. InChIKey : CJZGTCYPCWQAJB-UHFFFAOYSA-L |
| Apparence | solide blanc inodore[1] |
| Propriétés chimiques | |
Formule brute | C36H70CaO4 [Isomères] |
Masse molaire[2] | 607,017 ± 0,039 g/mol C 71,23 %, H 11,62 %, Ca 6,6 %, O 10,54 %, |
| Propriétés physiques | |
T° fusion | 140 à 160 °C[1] |
T° ébullition | 435 °C (décomposition) |
Solubilité | 2,2 mg·l-1 (eau, 20 °C)[1] |
Masse volumique | 1,12 g·cm-3 (15 °C)[1] |
T° d'auto-inflammation | 460 °C[1] |
| Écotoxicologie | |
LogP | 14,34[3] |
| Unités du SI et CNTP, sauf indication contraire. | |
modifier | |
Le stéarate de calcium est un carboxylate de calcium qui entre dans la composition de certains lubrifiants ou d'agents de surface (tensioactifs). Il se présente sous la forme d'une poudre blanche cireuse[4].
Production et formation |
Le stéarate de calcium résulte du réchauffement de l'acide stéarique, un acide gras, en présence d'oxyde de calcium :
- 2 C17H35COOH + CaO → (C17H35COO)2Ca + H2O.
C'est également le composant majeur du précipité blanc qui se forme lorsque du savon est mélangé à de l'eau calcaire[5].
On le trouve dans le commerce sous forme de suspension ou de poudre séchée. En tant qu'additif alimentaire il est signalé par le code générique E470.
Utilisations |
- Le stéarate de calcium est utilisé comme fluidifiant dans certaines poudres, notamment dans des aliments tels que les smarties, comme enrobant dans les bonbons durs tels que les sprees, et comme lubrifiant dans les crayons et les pastels.
- L'industrie du ciment utilise le stéarate pour limiter la désagrégation de produits à base de ciment dans la production de matériaux de construction, notamment les dalles ou les parpaings ; il sert également d'agent d'étanchéité[6].
- L'industrie du papier utilise le stéarate de calcium comme lubrifiant pour obtenir une surface glacée, et pour empêcher le dépôt de poussière et les cassures résultant du pliage des fibres de papier et de carton[7].
- Dans les plastiques, il sert d'agent capable de neutraliser ou d'absorber l'acide à des concentrations allant jusqu'à 1 000 ppm, de lubrifiant et d'agent de démoulage. Mélangé aux concentrés de colorant plastiques, il améliore l'humidification des pigments. Dans le PVC rigide, il accélère la fusion, améliore la plasticité et diminue le coefficient de dilatation thermique pendant le moulage.
- Dans l'industrie pharmaceutique et des produits de soins, il est utilisé pour faciliter le démoulage des cachets mais aussi comme anti-adhérent et comme gel.
- Le stéarate de calcium entre dans la composition de certains antimoussants.
Références |
Entrée « Calcium stearate » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 1er janvier 2013 (JavaScript nécessaire)
Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
(en) « Calcium stearate », sur ChemIDplus, consulté le 1er janvier 2013
Angelo Nora, Alfred Szczepanek, Gunther Koenen, Metallic Soaps, Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. DOI:10.1002/14356007.a16_361
Hermann Weingärtner, Water, Ullmann's Encyclopedia of Industrial Chemistry, 2007, Wiley-VCH, Weinheim. DOI:10.1002/14356007.a28_001
(en) Preventing Efflorescence, Portland Cement Association
(en) Brevet U.S. 5,527,383
- Portail de la chimie